静岡大学農学部/グリーン科学技術研究所 植物ストレスマネジメントコアの竹内 純 准教授の研究グループは、アブシシン酸(ABA)の代謝不活性化機構に着目してABAを構造改変することで、植物体内で代謝不活性化され難く、且つ太陽照射下でも安定なABAアゴニストを開発しました。
【研究のポイント】
・ABAは植物の環境ストレス耐性誘導を担っている植物ホルモンであり、長年農業への利用が期待されきたが、実用化は殆ど進んでいない。
・この主な要因は、ABAの光安定性の低さと植物内体での代謝不活性化の速さにある。
・本研究では、ABA受容体と代謝不活性化酵素の構造要求性の知見に基づいてABAを構造改変することで、上記2つのABAの弱点を同時に克服可能なABAアゴニストを設計・合成した。
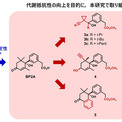
ABAの光安定性の低さは、側鎖ジエン酸の共役二重結合および環部のα,β-不飽和カルボニル基に由来します。これまでに当研究室では、光安定性の向上を目的として側鎖ジエン酸をフェニル酢酸に置換したABAアナログ(BP2A)、およびBP2Aのα,β-不飽和カルボニル基の4′位ケトンを還元したMe 1′,4′-trans-diol-BP2Aを創出してきました。しかし、植物体内で速やかに代謝不活性化されてしまうといった課題は残ったままでした。
そこで本研究では、BP2Aをリード化合物として代謝抵抗性を付与する方向で構造展開を行いました。その中で、BP2Aのシクロヘキセノン環にベンゼン環を融合させ、カルボキシ基をメチルエステルに置換した化合物5および6は、BP2Aよりも光に安定で、且つBP2Aよりも強いABA様の生物活性を示しました。
本研究で得られた研究成果は、環境ストレス耐性付与剤としてのABAアナログの農業利用を推進するものと期待されます。
なお、本研究成果は、2023年11月24日に国際雑誌「Organic & Biomolecular Chemistry」にオンライン掲載されました。
【研究者コメント】
本研究は、昨年度の修士修了生 朝倉悠さんが化合物の合成と活性評価に注力してくれた成果です。これまでに数多くのABA類縁化合物が合成されていますが、実用化における弱点であった光安定性の低さと植物体内での代謝不活性化の速さを同時に克服し得る化合物は存在しませんでした。化合物5/6はABAアナログの実用利用に向けた最初の一歩であると考えています。
【研究背景】
アブシシン酸(ABA)は、悪環境下での発芽抑制や乾燥耐性・塩耐性などを担う植物ホルモンであり、環境ストレス耐性付与剤としての農業利用が期待されています。しかし、圃場レベルでABAを植物に投与してもこの様な効果を発揮しないため、未だ実用化には至っていません。これはABAの効果持続性の低さに起因し、その主な要因はABAの光安定性の低さと植物内体での代謝不活性化の速さにあります。これまでに数多くのABA類縁化合が合成されてきましたが、未だ上記2つの弱点を同時に克服したABAアゴニストは存在しません。
ABAの光安定性の低さは、側鎖ジエン酸の共役二重結合および環部のα,β-不飽和カルボニル基に由来しています。そこで私たちは、先ず光安定性の向上を目的として、側鎖ジエン酸をフェニル酢酸に置換したABAアナログ(BP2A)、およびBP2Aのα,β-不飽和カルボニル基の4′位ケトンを還元したMe 1′,4′-trans-diol-BP2Aを開発しました(Takeuchi et al. J. Agric. Food Chem. 70, 869, 2022)。Me 1′,4′-trans-diol-BP2Aは、1週間屋外に放置しても全く分解されることのない高い光安定性と、ABAの1/3程度の生物活性を有し、実用性の高いABAアゴニストであると言えます。しかし、植物体内で速やかに代謝不活性化されてしまうといった課題は残ったままでした。そこで本研究では、BP2Aをリード化合物として代謝抵抗性を付与する方向に構造展開を行いました(下図)。
【研究の成果】
ABAは代謝不活性化酵素(CYP707A)によってシクロヘキセノン環上の8′位メチル基が水酸化された後、異性化して低活性なファゼイン酸へと変換されます。従って、代謝抵抗性を付与するには、シクロヘキセノン環を改変することが有効であると考えました。そこで先ず、BP2Aのシクロヘキセノン環をシアノシクロプロピル基に置換した化合物Me CP2As(下図; 3a-c)を合成しました。シアノシクロプロピル基は共役二重結合を含まないため、期待通り日光照射に対して高い安定性を示しました。しかし、生物活性はABAの1/10~1/30程度に低下しました。これは受容体に対する親和性が低下したためだと推測しています。
次に、BP2Aをメチルエステル化した後、8′位メチル基にアセチレンを導入し、4′位ケトンを還元したMe 8′-methylidyne-1′,4′-trans-diol-BP2A(4)、およびMe BP2Aのシクロヘキセノン環にベンゼン環を融合したMe tetralone-BP2A(5)を設計しました。また、化合物5の4′位ケトンを還元したMe diol-teralone-BP2A(6)も合成しました。日光照射試験において、化合物4-6はいずれもBP2Aよりも高い光安定性を有していることを確認しました。また、シロイヌナズナの種子発芽阻害を指標とした生物活性試験において、化合物5と6はBP2Aよりも強い阻害活性を示しました。さらにin vitro試験の結果から、化合物5/6の活性向上は、植物体内での代謝安定性に由来することが示唆されました。本研究成果は、ABAの実用化における弱点であった光安定性の低さと植物体内での代謝不活性化の速さを同時に克服しうるABAアゴニストの設計が可能であること示したことです。

【今後の展望と波及効果】
植物ホルモンやその類縁化合物は農業で広く利用されています。しかし、オーキシン、エチレン、ジベレリン、サリチル酸などに比べると、ABAの農業利用は限定的であり、特に乾燥ストレス耐性の付与といった、分かりやすくポジティブな機能を実用利用した例はこれまでにありません。本研究で開発した化合物5および6は、農業現場でABAを使用する際に障害となっていたABAの弱点を克服する一つの方法だと思います。今後は、シロイヌナズナ以外の農作物に対する効果や薬物動態を追究することで、ABAアナログの農業利用へと繋がることが期待されます。
【論文情報】
掲載誌名: Organic & Biomolecular Chemistry
論文タイトル: Synthesis and biological activity of photostable and persistent abscisic acid analogs
著者: Jun Takeuchi, Haruka Asakura, Yuri Ozasa, Motoki, Koide, Toshiyuki Ohnishi and Yasushi Todoroki
DOI: 10.1039/D3OB01518A
【研究助成】
竹内 純
日本学術振興会 科学研究助成事業 基盤研究B(22H02254)
【用語説明】
1.アブシシン酸(ABA)
生育に適さない悪環境下から植物を守ると同時に、生育を一時的に抑制する植物ホルモン。ABAの具体的な生理作用としては、種子の成熟と休眠の維持、アントシアニン生合成の促進(ブドウの果皮の着色促進にもABAが関与している)、および気孔閉鎖やそれに伴う乾燥耐性・低温耐性の誘導などが挙げられ、ABAは植物のストレスホルモンとして知られています。
2.アゴニスト
受容体に結合して、生体内物質と同様のシグナル伝達を作動させる薬剤。ABAまたはABAアゴニストが受容体と結合すると、受容体の立体配座が変化して標的タンパク質と相互作用出来るようになり、その結果、生体応答反応が誘導されます。
3.ABA代謝不活性化酵素
植物体内で不用となったABAを不活性化する酵素。ABAは主に、シトクロムP450(CYP707A)による8'位の水酸化と、UDPグルコシルトランスフェラーゼによる1位配糖体化によって不活性化されます。



コメント